Física Moderna
Escolha o assunto e comece seus estudos!
“A mente que se abre a uma nova ideia jamais voltará ao seu tamanho original.”
Albert Einstein
Física Moderna
LISTA 89 – FÍSICA MODERNA
01. (FUVEST) Em 20 de maio de 2019, as unidades de base do Sistema Internacional de Unidades (SI) passaram a ser definidas a partir de valores exatos de algumas constantes físicas. Entre elas, está a constante de Planck h, que relaciona a energia E de um fóton (quantum de radiação eletromagnética) com a sua frequência f na forma E = hf. A unidade da constante de Planck em termos das unidades de base do SI (quilograma, metro e segundo) é:
(A) kg m2/s
(B) kg s/m2
(C) m2s/kg
(D) kg s/m
(E) kg m2/s3
02. (SANTA CASA) Para explicar o fenômeno do efeito fotoelétrico, Einstein considerou que a luz é composta por fótons (partículas de luz) e que cada fóton transporta uma quantidade de energia, EF, dada pela expressão EF = h ⋅ f, sendo f a frequência da onda associada à luz e h a constante de Planck, de valor 6,6 × 10–34 J ∙ s. Um LED que emite 6,0 × 1018 fótons a cada minuto e cuja luz tem frequência 5,0 × 1014 Hz emite com potência igual a
(A) 3,0 × 10–3 W.
(B) 1,2 × 10–2 W.
(C) 5,6 × 10–2 W.
(D) 2,0 W.
(E) 3,3 × 10–2 W.
03. (FUVEST) O elétron e sua antipartícula, o pósitron, possuem massas iguais e cargas opostas. Em uma reação em que o elétron e o pósitron, em repouso, se aniquilam, dois fótons de mesma energia são emitidos em sentidos opostos. A energia de cada fóton produzido é, em MeV, aproximadamente,
a) 0,3
b) 0,5
c) 0,8
d) 1,6
e) 3,2
Note e adote:
Relação de Einstein entre energia (E) e massa (m): E = mc2
Massa do elétron = 9 × 10–31 kg
Velocidade da luz c = 3,0 × 108 m/s
1 eV = 1,6 × 10–19 J
1 MeV = 106 eV
No processo de aniquilação, toda a massa das partículas é transformada em energia dos fótons.
04. (UNESP) A sensibilidade visual de humanos e animais encontra–se dentro de uma estreita faixa do espectro da radiação eletromagnética, com comprimentos de onda entre 380 nm e 760 nm. É notável que os vegetais também reajam à radiação dentro desse mesmo intervalo, incluindo a fotossíntese e o crescimento fototrópico. A razão para a importância dessa estreita faixa de radiação eletromagnética é o fato de a energia carregada por um fóton ser inversamente proporcional ao comprimento de onda. Assim, os comprimentos de onda mais longos não carregam energia suficiente em cada fóton para produzir um efeito fotoquímico apreciável, e os mais curtos carregam energia em quantidade que danifica os materiais orgânicos.
(Knut Schmidt-Nielsen. Fisiologia animal: adaptação e meio ambiente, 2002. Adaptado.)
A tabela apresenta o comprimento de onda de algumas cores do espectro da luz visível:
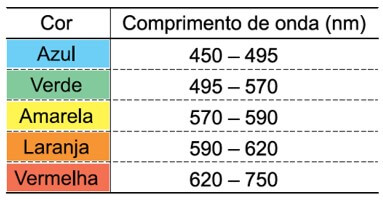
Sabendo que a energia carregada por um fóton de frequência f é dada por E = h × f, em que h = 6,6 × 10–34 J.s, que a velocidade da luz é aproximadamente c = 3 × 108 m/s e que 1 nm = 10–9 m, a cor da luz cujos fótons carregam uma quantidade de energia correspondente a 3,96 × 10–19 J é
(A) azul.
(B) verde.
(C) amarela.
(D) laranja.
(E) vermelha.
05. (FAMERP) Em certos
exames de medicina nuclear, uma substância radioativa é administrada ao
paciente que, posteriormente, é acomodado em um aparelho. Quando o elemento
radioativo decai, os detectores do aparelho captam parte dos fótons emitidos.
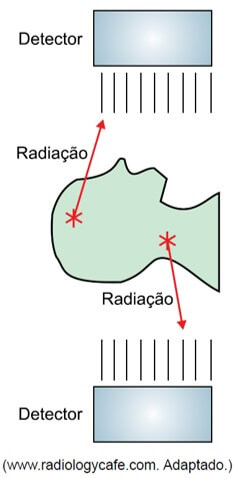
Sabe-se que a energia associada a um fóton está relacionada com a frequência da radiação pela expressão Ef = h · f, sendo h a constante de Planck, cujo valor é 6,63 × 10 – 34 J·s. Suponha que o elemento radioativo utilizado em um desses exames seja o tecnécio-99m, que emite radiação cujos fótons têm energia associada de 2,24 × 10–14 J, e considere os detectores de radiação sensíveis às faixas de frequência indicadas na tabela.
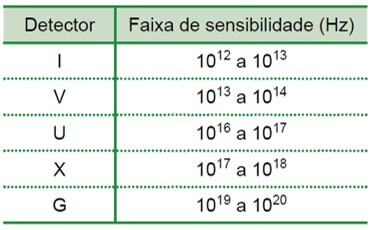
Para que possam captar os fótons emitidos pelo tecnécio-99m, os detectores utilizados no aparelho devem ser do tipo
(A) X.
(B) G.
(C) V.
(D) I.
(E) U.
06. (FUVEST) A energia irradiada pelo Sol provém da conversão de massa em energia durante reações de fusão de núcleos de hidrogênio para produzir núcleos de hélio. Atualmente, essas reações permitem ao Sol emitir radiação luminosa a uma potência de aproximadamente 4 x 1026 W. Supondo que essa potência tenha sido mantida desde o nascimento do Sol, cerca de 5 x 109 anos atrás, a massa correspondente àquela perdida pelo Sol até hoje é mais próxima de
a) 107 kg.
b) 1017 kg.
c) 1027 kg.
d) 1037 kg.
e) 1047 kg.
Note e adote:
Velocidade da luz no vácuo: 3 x 108 m/s.
Considere que um ano tem cerca de 3 x 107 s.
07. (FUVEST) Alguns equipamentos de visão noturna têm seu funcionamento baseado no efeito fotoelétrico, uma das primeiras descobertas que contribuíram para o surgimento da mecânica quântica. Nesses equipamentos, fótons de frequência f emitidos por um objeto incidem sobre uma superfície metálica. Elétrons são então liberados da superfície e acelerados por um campo elétrico. Em seguida, o sinal eletrônico é amplificado e produz uma imagem do objeto. Diferentemente do que a física clássica prevê, apenas os elétrons com energia hf acima de uma certa energia mínima E0 são liberados da superfície metálica. Considerando a incidência de fótons com frequência da ordem de 1014 Hz, a ordem de grandeza do valor limite de E0 para que o equipamento funcione deve ser:
(A) 10−50 J
(B) 10−40 J
(C) 10−30 J
(D) 10−20 J
(E) 10−10 J
Note e adote:
Constante de Planck: h = 6,63 × 10−34 J.s
08. (UNESP) O efeito fotoelétrico é um processo em que ocorre a emissão de elétrons por uma placa metálica, chamados fotoelétrons, quando a radiação eletromagnética incide sobre ela com uma quantidade de energia suficiente para removê-los da superfície da placa. A quantidade mínima dessa energia que remove cada elétron é chamada função trabalho do metal (Φ). No estudo desse efeito, considera-se que a energia (ε) associada a um fóton de determinada radiação que se propaga com frequência f é dada pela expressão ε = h × f, em que h é uma constante positiva. Nesse processo, essa energia é totalmente absorvida por um elétron ligado à placa, sendo parte utilizada para removê-lo do metal e o restante transformada em energia cinética desse fotoelétron (Ecin = ε – Φ).
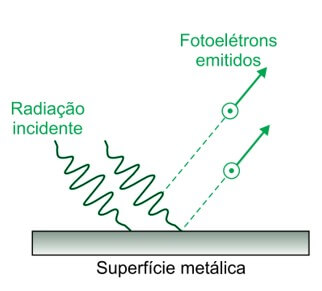
A tabela apresenta as funções trabalho do sódio e do alumínio, expressas em joules.
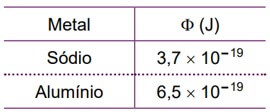
Considere que uma radiação ultravioleta de comprimento de onda λ = 4 × 10–7 m, propagando-se no vácuo, incida sobre duas placas, uma feita de sódio e outra de alumínio. Sendo a velocidade da luz no vácuo c = 3 × 108 m/s e adotando-se h = 6,4 × 10–34 J · s, nessa situação somente a placa de
(A) alumínio emitirá fotoelétrons, cada um com 2,0 × 10–19 J de energia cinética.
(B) alumínio emitirá fotoelétrons, cada um com 2,4 × 10–19 J de energia cinética.
(C) sódio emitirá fotoelétrons, cada um com 2,4 × 10–19 J de energia cinética.
(D) sódio emitirá fotoelétrons, cada um com 1,1 × 10–19 J de energia cinética.
(E) alumínio emitirá fotoelétrons, cada um com 1,1 × 10–19 J de energia cinética.
09. (SANTA CASA 2023) Albert Einstein é muito conhecido por ter elaborado a Teoria da Relatividade, mas o trabalho que lhe rendeu o Prêmio Nobel de Física de 1921 foi sobre o efeito fotoelétrico. Esse efeito consiste
(A) na emissão de elétrons por uma superfície metálica quando é atingida por radiação eletromagnética.
(B) na emissão de luz pelos LEDs quando são percorridos por corrente elétrica.
(C) na emissão de luz por um metal aquecido, como ocorre nas lâmpadas incandescentes.
(D) na emissão de elétrons pelo núcleo atômico (radiação beta menos) quando é atingido por radiação luminosa.
(E) na emissão de luz por um gás quando é atingido por elétrons, como ocorre nas lâmpadas fluorescentes.
10. (FAMERP 2023) No modelo do átomo de hidrogênio proposto por Bohr, os elétrons só podem ocupar certos estados estacionários e a energia de cada um desses estados é dada, em elétron-volts (eV), por ![]() , sendo n o número quântico principal do estado considerado. Apenas ao passar de um estado para outro o elétron absorve ou emite uma quantidade de energia que corresponde à diferença entre as energias desses dois estados. Nesse modelo, quando um elétron faz uma transição do estado n = 2 para o estado n = 3, ele absorve uma quantidade de energia que é de, aproximadamente,
, sendo n o número quântico principal do estado considerado. Apenas ao passar de um estado para outro o elétron absorve ou emite uma quantidade de energia que corresponde à diferença entre as energias desses dois estados. Nesse modelo, quando um elétron faz uma transição do estado n = 2 para o estado n = 3, ele absorve uma quantidade de energia que é de, aproximadamente,
(A) 1,89 eV.
(B) 1,51 eV.
(C) 2,72 eV.
(D) 3,40 eV.
(E) 4,53 eV.
Respostas
1- A
2- E
3- B
4- B
5- B
6- C
7- D
8- D
9- A
10- A
